Esta cifra supone un ligero incremento con respecto al año pasado; las pruebas se realizarán del 2 al 4 de junio en las diferentes sedes
Investigadores de Salamanca identifican cómo una proteína puede frenar el tumor pero favorecer la metástasis
El trabajo ha sido desarrollado por científicos del Centro de Investigación del Cáncer, que han descubierto el papel de la proteína C3G en el linfoma de células B
Un equipo de investigadores del Centro de Investigación del Cáncer de Salamanca ha descubierto que la proteína C3G desempeña un papel dual en el linfoma de células B, un tipo de cáncer hematológico. Según el estudio, su hiperactivación puede frenar el crecimiento del tumor, pero al mismo tiempo aumenta la capacidad de las células cancerosas para migrar y generar metástasis.
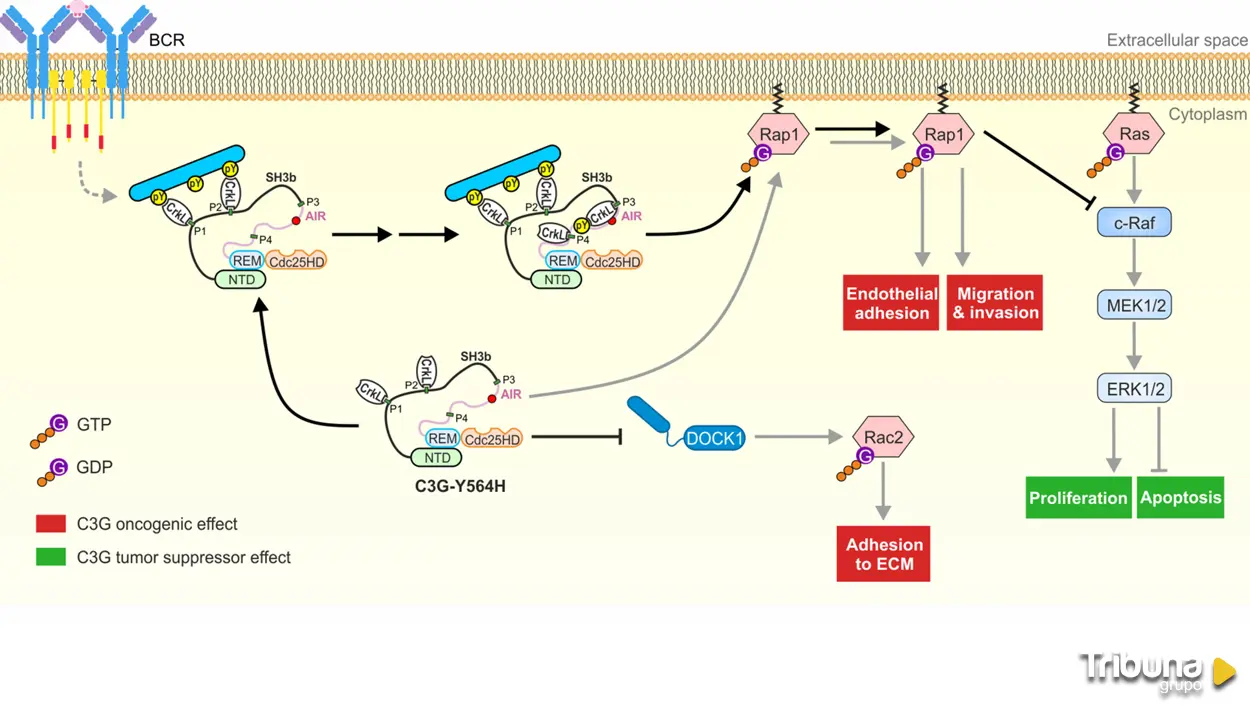
La proteína C3G actúa como un 'interruptor' molecular que regula la activación de Rap1, una molécula clave en procesos celulares como la adhesión, el crecimiento o el movimiento de las células. Sin embargo, en algunos pacientes con linfoma no Hodgkin se ha detectado una mutación que elimina el control natural de esta proteína y provoca que permanezca activada de forma constante.
Para analizar las consecuencias de esta alteración genética, los investigadores recrearon la mutación en células de linfoma mediante la técnica de edición genética CRISPR. Los experimentos mostraron que la mutación provoca una activación permanente de Rap1, lo que reduce la proliferación celular al disminuir la actividad de la proteína c-Raf.
En los modelos celulares analizados, las células con esta mutación crecieron hasta un 50% menos en 72 horas y mostraron una mayor sensibilidad al estrés celular, debido a la disminución de Bcl-xL, una proteína que protege frente a la muerte celular.
Sin embargo, el estudio también reveló que esta misma mutación modifica el comportamiento migratorio de las células tumorales. La alteración reduce la actividad de Rac2, una proteína implicada en la adhesión de las células sanguíneas a su entorno. Como consecuencia, las células mutadas se adhieren menos a su entorno, pero aumentan su capacidad de desplazamiento y de diseminación hacia otros tejidos.
Confirmación en modelos animales
Para comprobar estos resultados en condiciones más cercanas a la enfermedad real, los científicos realizaron experimentos con ratones. En estos modelos animales se introdujeron células tumorales con la mutación en la proteína C3G.
Tras 21 días, los análisis mostraron que los animales desarrollaron un mayor número de focos metastásicos en el hígado en comparación con los controles, lo que confirma el aumento de la capacidad invasiva de las células mutadas.
Según explica la investigadora Alba Morán-Vaquero, primera autora del trabajo, los resultados "validan el doble efecto de C3G: actúa como supresor del crecimiento tumoral primario a través de Rap1, pero también puede promover la metástasis al reducir la adhesión celular".
El estudio ha sido realizado por investigadores del Centro de Investigación del Cáncer, un instituto mixto en el que participan el Consejo Superior de Investigaciones Científicas, la Universidad de Salamanca y la Fundación para la Investigación del Cáncer de la Universidad de Salamanca. En el proyecto también han participado el Instituto de Investigación Biomédica de Salamanca y la Universidad de Leiden.
La investigación ha contado con financiación de la Junta de Castilla y León, el Ministerio de Ciencia, Innovación y Universidades, el Instituto de Salud Carlos III, la Fundación Científica de la AECC y fondos europeos FEDER.
El Consejo de Gobierno ha aprobado también los itinerarios sucesivos de ingeniería y ha definido el peso de las asignaturas de la PAU
La USAL cuenta en esta edición con 13 indicadores de alto rendimiento y vuelve a situarse como la institución académica más destacada de Castilla y León
La Universidad de Salamanca ha editado un facsímil con un relato del escritor bilbaíno, considerado la primera obra de ciencia ficción española